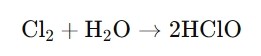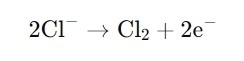Хлорноватистая кислота: сильная или слабая?
Введение
Когда мы думаем о кислотах, мы часто представляем себе что-то, что может разъедать металл или вызвать ожоги кожи. А как насчет хлорноватистой кислоты (HClO)? Оно сильное или слабое?
В этой обширной статье мы исследуем свойства HClO, его преимущества, применение и то, как он играет жизненно важную роль в нашей повседневной жизни.
Присоединяйтесь к нам, когда мы погрузимся в химию HClO и узнаем, почему она заслуживает нашего внимания.
Что такое хлорноватистая кислота?
Хлорноватистая кислота — это простое соединение, образующееся при растворении газообразного хлора в воде. Это ключевой игрок в различных приложениях, особенно в санитарии и дезинфекции.
·Химический состав: HClO состоит из одного атома водорода, одного атома хлора и одного атома кислорода.
·Формирование: Вы создаете HClO, когда смешиваете газообразный хлор с водой. Реакцию можно резюмировать следующим образом:
Это показывает, как хлор взаимодействует с водой с образованием хлорноватистой кислоты.
Электролиз: производство хлорноватистой кислоты
Одним из наиболее эффективных методов получения хлорноватистой кислоты (HClO) является электролиз. Этот процесс включает пропускание электрического тока через раствор соленой воды, в результате чего образуется HClO вместе с другими побочными продуктами. Давайте углубимся в то, как работает этот процесс и его значение.
Что такое электролиз?
Электролиз — это химический процесс, в котором используется электрическая энергия для запуска неспонтанной реакции. В случае производства HClO оно включает электролиз раствора хлорида натрия (NaCl), широко известного как физиологический раствор.
Процесс электролиза
1.Приготовление раствора:
· Смешайте воду с небольшим количеством соли (хлорида натрия). Это создает солевой раствор, который будет проводить электричество.
2.Установка электролиза:
· Солевой раствор помещается в электролитическую ячейку, содержащую два электрода: анод (положительный электрод) и катод (отрицательный электрод).
3.Применение электрического тока:
· При подаче электрического тока на электродах происходит ряд электрохимических реакций.
4.Химические реакции:
· На аноде ионы хлорида (Cl⁻) окисляются до газообразного хлора (Cl₂):
· На катоде вода восстанавливается с образованием газообразного водорода (H₂) и гидроксид-ионов (OH⁻):
5.Образование хлорноватистой кислоты:
· Газообразный хлор, образующийся на аноде, реагирует с водой с образованием хлорноватистой кислоты:
· Полученный раствор содержит HClO и другие соединения, в зависимости от условий электролиза.
Преимущества электролиза для производства HClO
1.Генерация на месте:
· Электролиз позволяет производить HClO на месте, обеспечивая свежесть и снижая потребность в хранении.
2.Настраиваемые концентрации:
· Пользователи могут регулировать концентрацию HClO, изменяя концентрацию соли и продолжительность электролиза.
3.Экологичный:
· В процессе образуется минимальное количество отходов, а первичные побочные продукты (вода и соль) экологически безопасны.
4.Экономичный:
· Производство HClO посредством электролиза может быть более экономичным, чем покупка готовых растворов, особенно для крупномасштабного применения.
Применение электролитического HClO
Хлорноватистая кислота, получаемая в результате электролиза, имеет различные применения, что делает ее универсальным решением в различных отраслях промышленности.
1.Настройки здравоохранения
В больницах и клиниках электролитическая HClO используется для дезинфекции поверхностей и медицинского оборудования. Его эффективность против широкого спектра патогенов помогает контролировать инфекцию.
2.Пищевая промышленность
На предприятиях пищевой промышленности электролитическая HClO используется для дезинфекции оборудования и поверхностей, обеспечивая безопасность пищевых продуктов за счет минимизации микробного загрязнения.
3.Очистка воды
Муниципальные водоочистные сооружения используют HClO, полученную в результате электролиза, для дезинфекции питьевой воды и сточных вод, обеспечивая безопасную воду для населения.
4.Бытовая Уборка
Многие бытовые чистящие и дезинфицирующие средства теперь содержат электролитическую HClO, обеспечивающую безопасное и эффективное средство для дезинфекции поверхностей в доме.
Понимание кислотности
Чтобы определить, является ли HClO сильным или слабым, нам нужно понять понятие кислотности в химии.
Определение кислот
В химии кислоты определяют по их способности отдавать протоны (ионы H⁺) другим веществам.
·Теория Брёнстеда-Лоури: Согласно этой теории, кислота – это любое вещество, способное отдавать протон.
·Теория Аррениуса: Эта теория утверждает, что кислота — это вещество, которое увеличивает концентрацию ионов водорода в водном растворе.
Используя эти определения, мы можем оценить поведение хлорноватистой кислоты.
Является ли HClO сильной кислотой?
Давайте выясним, что делает кислоту сильной или слабой.
·Сильные кислоты: Сильные кислоты полностью диссоциируют в воде. Это означает, что они выделяют все свои ионы водорода в раствор.
·Поведение HClO: Хлорноватистая кислота лишь частично диссоциирует в воде, высвобождая некоторые, но не все ионы водорода. Как результат,мы относим ее к слабым кислотам.
Это различие имеет решающее значение, поскольку сила кислоты влияет на ее реакционную способность и применение.
pH хлорноватистой кислоты
Шкала pH показывает, насколько кислым или щелочным является раствор: от 0 (очень кислый) до 14 (очень щелочной).
·Типичный pH HClO: Хлорноватистая кислота обычно имеет pH от 5 до 6,5, что указывает на умеренную кислотность.
Почему pH имеет значение?
Понимание pH HClO помогает нам оценить, как он взаимодействует в различных средах.
·Влияние на эффективность: Эффективность HClO как дезинфицирующего средства увеличивается в определенных диапазонах pH. Например, более низкие уровни pH усиливают его антимикробные свойства.
·Применение в очистке воды: Поддержание правильного уровня pH в бассейнах гарантирует, что HClO останется эффективным в уничтожении вредных микроорганизмов.
Преимущества хлорноватистой кислоты
Что делает HClO особенным? Вот некоторые из его ключевых преимуществ:
1.Эффективное дезинфицирующее средство: HClO известен своей способностью убивать бактерии и вирусы. Это делает его популярным выбором для санитарии в различных условиях.
2.Безопасно для использования: В отличие от более сильных кислот, HClO безопасен в обращении и не раздражает кожу. Это особенно важно в медицинских учреждениях.
3.Экологичный: HClO распадается на безвредные вещества, сводя к минимуму свое воздействие на окружающую среду. Он разлагается на соль и воду, что делает его экологически безопасным выбором.
4.Универсальные приложения: HClO находит применение во многих отраслях промышленности: от бытовых чистящих средств до очистки воды.
5.Нетоксичный: Он представляет минимальный риск для здоровья человека и безопасен для использования в помещениях для приготовления пищи.
Как работает HClO?
Давайте рассмотрим механизм эффективности HClO в качестве дезинфицирующего средства.
Механизм действия
·Проникновение: HClO проникает в микробные клетки, повреждая их структуры и эффективно убивая их.
·Окислительный стресс: HClO вызывает окислительный стресс у бактерий и вирусов, приводящий к гибели клеток.
·Широкий спектр эффективности: HClO эффективен против широкого спектра патогенов, включая бактерии, вирусы и грибки. Эта универсальность делает его неоценимым для санитарной обработки.
Формула гипохлорит-иона
Понимание гипохлорит-иона (ClO⁻) расширяет наше понимание HClO.
·Сопряженная база: Ион гипохлорита (ClO⁻) представляет собой сопряженное основание HClO. Когда HClO отдает протон, он становится ClO⁻.
·Роль в химии: Этот ион также проявляет дезинфицирующие свойства, особенно при очистке воды. Его часто используют в форме гипохлорита натрия (NaClO) в бытовых отбеливателях.
Ионная стабильность гипохлорита
·Факторы стабильности: На стабильность ClO⁻ могут влиять pH и температура. При более низких уровнях pH ClO⁻ более стабилен, что способствует эффективности HClO в качестве дезинфицирующего средства.
Практическое применение хлорноватистой кислоты
HClO находит применение во многих продуктах и приложениях. Вот некоторые распространенные варианты использования:
1.Бытовые чистящие средства: Многие дезинфицирующие и дезинфицирующие средства содержат HClO из-за его мощных антибактериальных свойств.
2.Очистка воды: Это основной элемент поддержания чистоты и безопасности плавательных бассейнов. HClO эффективно убивает вредные патогены, обитающие в воде бассейна.
3.Здравоохранение: HClO, используемый при лечении ран и в хирургических учреждениях, помогает предотвратить инфекции благодаря своим антибактериальным свойствам.
4.Пищевая промышленность: HClO часто используется для дезинфекции поверхностей и оборудования, контактирующих с пищевыми продуктами, обеспечивая безопасность пищевых продуктов.
5.Сельское хозяйство: Фермеры используют HClO для дезинфекции оборудования и борьбы с болезнетворными микроорганизмами в поливной воде.
6.Ветеринарная помощь: Используется в ветеринарии для дезинфекции ран и хирургических инструментов.
Как получить хлорноватистую кислоту
Мы часто полагаемся наГенератор HOClдля эффективного производства HClO. Вот как это работает:
1.Смешайте воду и соль: Начните с объединения воды и соли. Эта смесь необходима для процесса электролиза.
2.Применить электролиз: Генератор подает электрический ток для производства HClO. Этот процесс облегчает реакцию между ионами хлора и водой.
3.Храните решение: Вы можете сохранить сгенерированное решение для использования в будущем. Обеспечьте надлежащие условия хранения для поддержания его эффективности.
Преимущества использования генератора HOCl
·Производство на месте: Производство HClO на месте обеспечивает свежесть и эффективность, уменьшая необходимость в транспортировке и хранении.
·Экономичный: Производство HClO с помощью генератора может быть более экономичным, чем покупка готовых растворов.
·Пользовательские концентрации: Пользователи могут регулировать концентрацию HClO в зависимости от конкретных потребностей, что делает его универсальным для различных применений.
Сравнение хлорноватистой кислоты с другими кислотами
Как HClO сочетается с другими кислотами?
Сравнение с сильными кислотами
·Безопасность: В отличие от сильных кислот, таких как соляная кислота (HCl), HClO представляет меньший риск для здоровья и безопасности человека.
·Универсальность: HClO подходит для использования в чувствительных средах, таких как приготовление пищи и здравоохранение.
По сравнению с другими слабыми кислотами
·Эффективность: HClO превосходит некоторые слабые кислоты по антимикробной эффективности. Например, уксусная кислота (уксус) обладает более слабой дезинфицирующей способностью по сравнению с HClO.
Важность правильного использования
Правильное использование HClO максимизирует его преимущества. Вот несколько советов:
1.Следуйте рекомендациям: Всегда придерживайтесь рекомендуемых концентраций в целях безопасности. Чрезмерное или неправильное использование может привести к неэффективной дезинфекции.
2.Мониторинг уровня pH: Поддержание pH в оптимальном диапазоне обеспечивает эффективность HClO. Регулярное тестирование может помочь поддерживать желаемый уровень pH.
3.Храните правильно: Храните HClO в темных, прохладных местах для сохранения стабильности. Воздействие света и тепла может ухудшить его эффективность.
Развенчание мифов о хлорноватистой кислоте
Существует много заблуждений относительно HClO. Давайте рассмотрим некоторые:
·Миф 1: HClO опасен.
·Факт: HClO безопаснее многих сильных кислот и имеет низкий потенциал раздражения.
·Миф 2: Все дезинфицирующие средства одинаковы.
·Факт: HClO уникален благодаря своей эффективности и безопасности.
·Миф 3: HClO имеет резкий запах.
·Факт: Хлорноватистая кислота имеет более слабый запах по сравнению с газообразным хлором, что делает ее более приятной в использовании.
Реальные примеры использования HClO
В здравоохранении
Больницы и клиники используют HClO для дезинфекции поверхностей и инструментов. Это помогает предотвратить инфекции, связанные со здравоохранением, защищая как пациентов, так и персонал.
В пищевой промышленности
Производители продуктов питания используют HClO для дезинфекции оборудования и поверхностей. Такая практика помогает обеспечить безопасность пищевых продуктов и продлевает срок их хранения за счет снижения микробного загрязнения.
На водоочистных сооружениях
Муниципальные водоочистные сооружения часто используют HClO для дезинфекции.
Ссылки
1.Центры по контролю и профилактике заболеваний (CDC)- Дезинфекция хлорноватистой кислотой.Руководство CDC по хлорноватистой кислоте
2.Журнал экологических наук и здоровья- Роль HClO в очистке воды. Журнал наук об окружающей среде
3.Химия LibreTexts- Сила кислоты и диссоциация. LibreTexts Химия
4.Агентство по охране окружающей среды (EPA)- Руководство по хлорированию и хлорноватистой кислоте.Рекомендации Агентства по охране окружающей среды
5.Всемирная организация здравоохранения (ВОЗ)- Вода, санитария и гигиена: Руководство по дезинфекции.Рекомендации ВОЗ по дезинфекции
6.Международный журнал экологических исследований и общественного здравоохранения- Безопасность и эффективность хлорноватистой кислоты. АЙЕРФ
7.Американский журнал инфекционного контроля- Антимикробные свойства хлорноватистой кислоты.АДЖИК
8.Журнал защиты пищевых продуктов- Использование хлорноватистой кислоты в обеспечении безопасности пищевых продуктов. Журнал защиты пищевых продуктов
9.Журнал госпитальной инфекции- Хлорноватистая кислота как дезинфицирующее средство в здравоохранении.Журнал госпитальной инфекции
10.Пищевая и химическая токсикология- Токсикология хлорноватистой кислоты и ее применение. Пищевая и химическая токсикология